Então, afinal o que é um gás?
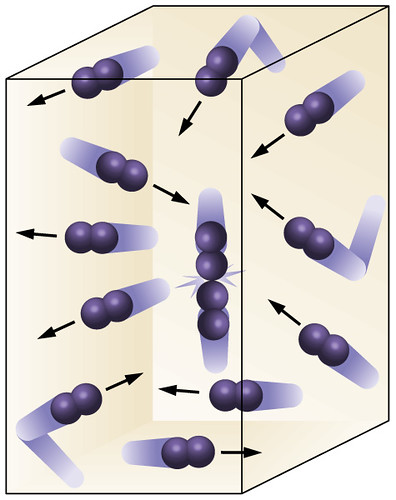 |
| No modelo cinético dos gases, as moléculas são consideradas como pontos infinitesimais que viajam em linhas retas até que eles sofrem colisões instantâneas. Fonte: http://quimicafv.blogspot.com.br/2012/02/modelo-cinetico-molecular.html |
Bem, ainda precisamos de muitas definições e conceitos que veremos nas próximas postagens. Todavia, já podemos definir um gás da maneira como este é definido pela Teoria Cinética Molecular dos Gases, ou modelo cinético dos gases.
Lembrete: Todo modelo é uma construção imaginária que incorpora apenas as características consideradas importantes para a descrição do sistema físico em questão. Estas características são selecionadas intuitivamente ou por conveniência matemática. A validade de um modelo é determinada pela experimentação.
O modelo da teoria cinética para um gás ideal se baseia nas seguintes hipóteses:
- O gás é constituído de massa m em movimento aleatório incessante.
- As moléculas do gás em questão estão bastante distanciadas, existindo um imenso vazio entre elas.
- Um gás dentro de um recipiente descreve um movimento retilíneo uniforme. Os choques entre as moléculas do gás e a parede do recipiente e entre as próprias moléculas (colisões) são completamente elásticos, isto é, não há perda de energia cinética durante estes choques ou colisões.
- Não há interação ou atração entre as moléculas dos gases, sedo que as moléculas de gás só interagem quando em contato nas colisões elásticas, que não são frequentes.
Uma colisão elástica é uma colisão em que a energia cinética de translação total se conserva (isto é, permanece constante).
O vídeo abaixo, apesar de estar em espanhol ilustra bem esse modelo cinético:
Veremos nas próximas postagens que estes postulados explicam propriedades importantes dos gases: a pressão, a relação entre esta e a temperatura ou o volume, as velocidades de difusão e efusão de gases e ainda mais.
Fonte:
Atkins, P. W. (Peter William), 1940 - Atkins, físico-química, v.2/ Peter Atkins, Julio de Paula.
O estado gasoso: http://www.qmc.ufsc.br/quimica/pages/aulas/gas_page1.html
Nenhum comentário:
Postar um comentário