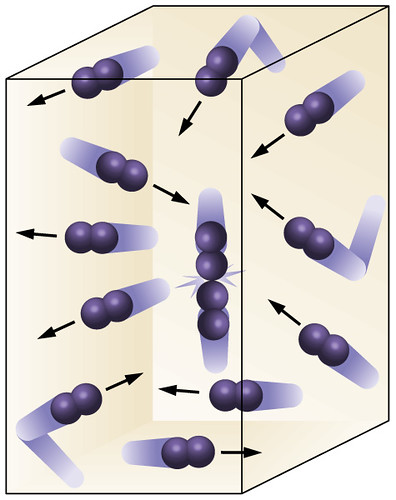
A lei de Boyle
Descreve o comportamento do gás ideal quando se mantém sua temperatura constante (transformação isotérmica).
Considere um recipiente com tampa móvel que contém certa quantidade de gás. Aplica-se lentamente uma força sobre essa tampa, pois desse modo não alteraremos a temperatura do gás. Observaremos um aumento de pressão junto com uma diminuição do volume do gás, ou seja, quando a temperatura do gás é mantida constante, pressão e volume são grandezas inversamente proporcionais.
Essa lei pode ser expressa matematicamente do seguinte modo:
Onde k é uma constante que depende da temperatura, da massa e da natureza do gás. A transformação descrita é representada na figura a seguir em um diagrama de pressão por volume:
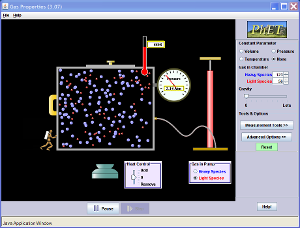
Vejamos agora a seguinte animação:
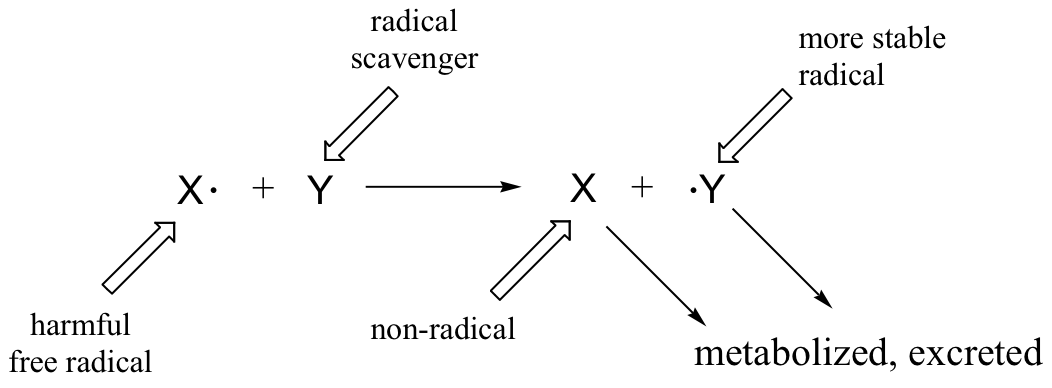 |
| Lei de Boyle para uma caixa com variação de volume. |
Consideramos a caixa cheia de moléculas de gás em movimento. As partículas têm a mesma energia (temperatura) durante todo o movimento. À medida que a caixa diminui, as partículas passam a ter uma pequena distância a percorrer antes que colidem com as paredes e, portanto, o tempo entre as colisões fica cada vez menor. Num dado período de tempo as partículas batem mais nas paredes, o que resulta em uma maior quantidade de pressão. A quantidade de mols é claramente constante, como não estamos acrescentando ou subtraindo partículas da caixa. Outra forma de olhar para isto é que, o aumento da pressão impulsiona as partículas entre si. Estas partículas compactadas agora ocupam menos volume. A fim de comparar a pressão de um gás com um outro ou de o volume variar, podemos combinar as equações de P1V1 = k e P2V2 = k. Porque k é uma constante para ambos os valores de pressão e de volume,
P1V1 = P2V2
A lei de Charles
Neste caso, mantém-se o volume constante.
Este é um experimento que você pode fazer em casa: encha um balão (de festa) até metade de sua capacidade. Depois, prepare duas bacias (ou panelas) com água gelada (água+gelo) e água quente (fervente). A seguir, mergulhe o balão na água gelada. Observe seu volume. Repentinamente, transfira o balão para o recipiente com água quente, e observe o volume deste.
A lei de Charles descreve essa situação, ou seja, em uma transformação isométrica (volume constante), a pressão e a temperatura serão grandezas diretamente proporcionais. Matematicamente, a lei de Charles é expressa da seguinte forma:
Onde k é uma constante que depende do volume, da massa e da natureza do gás.
O gráfico da pressão em função da temperatura absoluta fica da seguinte forma:
Vamos entender melhor observando a seguinte animação:
 |
| Quanto maior for a temperatura e velocidade da bola vermelha significa que esta abrange mais volume em um determinado momento. |
Ambas as partículas deixam a retornar e, ao mesmo tempo, mas desde que a bola vermelha viaje uma distância mais longa, deve-se mover mais rápido e terá mais energia. Você pode ver um aumento da energia cinética e temperatura, assim como o volume. Também note que a pressão permanece constante. Ambas as caixas têm o mesmo número de colisões num determinado período de tempo. De acordo com a Lei de Charles, você pode escrever a seguinte equação combinada,
V1/T1 = V2/T2
A lei de Gay-Lussac
A lei de Gay-Lussac nos mostra o comportamento de um gás quando é mantida a sua pressão constante e variam-se as outras duas grandezas: temperatura e volume. Dessa vez vamos considerar novamente um gás em um recipiente de tampa móvel. Dessa vez, nós aqueceremos o gás e deixaremos a tampa livre, como mostra a figura abaixo. Feito isso, veremos uma expansão do gás junto com o aumento de temperatura. O resultado será uma elevação da tampa e, consequentemente, um aumento de volume. Lembre-se que a pressão sobre a tampa - nesse caso a pressão atmosférica - se mantém constante.
Essa lei é expressa matematicamente da seguinte forma:
Onde k é uma constante que depende da pressão, da massa e da natureza do gás.
Em um gráfico do volume em função da temperatura, teremos o seguinte resultado:
A Equação de Clapeyron
A equação de Clapeyron pode ser entendida como uma síntese dessas três leis acima descritas, relacionando pressão, temperatura e volume.
Considerando que o número de moléculas influencia na pressão exercida pelo gás, ou seja, a pressão também depende diretamente da massa do gás, Paul Emile Clapeyron (1799-1844) estabeleceu uma relação entre as variáveis de estado com a seguinte expressão matemática:
Onde n é o número de mols e R é a constante universal dos gases perfeitos. Essa constante pode assumir os seguintes valores:
A equação geral dos gases perfeitos
Considere uma determinada quantidade de gás ideal confinado em um recipiente onde se pode variar a pressão, o volume e a temperatura, mas mantendo-se a massa constante, ou seja, sem alterar o número de mols, como ilustra a figura (1) abaixo:
Assim, a partir da equação de Clapeyron, podemos estabelecer a seguinte relação:
Como foi descrito o número de mols n e R são constantes. Conclui-se então que:
Assim, para os dois casos ilustrados na figura acima, temos que:
Observando que essas duas equações dão o mesmo resultado, e que portanto elas são iguais, então, podemos obter a seguinte equação final, que é conhecida como a equação geral dos gases perfeitos:
Referências: